CIRUGIA LAPAROSCOPICA
La laparoscopia es una técnica exploratoria o diagnóstica que también se emplea para realizar intervenciones quirúrgicas a través de pequeñas incisiones, lo que permite que el paciente se recupere antes y mejor.
Las técnicas mínimamente invasivas como la laparoscopia han permitido que el postoperatorio de los pacientes sea más corto y menos doloroso, por lo que no necesitan tomar tantas pastillas para el dolor y los hospitales se ahorran costes al ser la estancia hospitalaria más corta. También disminuyen el número de infecciones en el postoperatorio.
Ventajas de la Cirugía Laparoscópica:
• Pequeñas y estéticas incisiones.
• Menos dolor post operatorio.
• Recuperación más rápida, que permite incorporarse antes a la vida diaria.
• Menor incidencia de adherencias postoperatorias (cicatrices internas), que pueden provocar en algunas pacientes dolor y obstrucciones intestinales en algún momento de su vida.
• Mayor visualización de la cavidad abdominal.
• Posibilidad de realizar varios procedimientos quirúrgicos a través de las mismas incisiones.
• Menor tiempo de hospitalización. Es posible dar el alta al día siguiente de la intervención.
• Mejores resultados estéticos: mínima cicatriz abdominal, prácticamente invisible.
• Pequeñas y estéticas incisiones.
• Menos dolor post operatorio.
• Recuperación más rápida, que permite incorporarse antes a la vida diaria.
• Menor incidencia de adherencias postoperatorias (cicatrices internas), que pueden provocar en algunas pacientes dolor y obstrucciones intestinales en algún momento de su vida.
• Mayor visualización de la cavidad abdominal.
• Posibilidad de realizar varios procedimientos quirúrgicos a través de las mismas incisiones.
• Menor tiempo de hospitalización. Es posible dar el alta al día siguiente de la intervención.
• Mejores resultados estéticos: mínima cicatriz abdominal, prácticamente invisible.
Complicaciones de la Cirugía Laparoscópica :
• Anestésicas: la anestesia general es muy segura. Una consulta previa con el anestesiólogo puede dar mayor tranquilidad a la paciente.
• Hemorragia: el sangrado excesivo puede presentarse en el momento de la colocación de las cánulas o durante el procedimiento quirúrgico en sí, pero es muy poco frecuente. La paciente debe ser evaluada en cuanto a su grupo sanguíneo y nivel de Hemoglobina en sangre previo a la cirugía.
• Lesiones Gastrointestinales : pueden presentarse en 1 de cada 500 cirugías laparoscópicas, y son mas frecuentes en pacientes con antecedentes de cirugía intestinal e incisiones a nivel de la línea media. Esta es una complicación seria que requiere cirugía mayor y control estricto.
• Lesiones Urológicas : pueden presentarse en el 0.1% de las histerectomías. Las lesiones de la vejiga y uréteres son mas frecuentes en pacientes con antecedente de cesárea y endometriosis pélvica severa por lo que estas pacientes requieren de un cuidado especial durante el procedimiento quirúrgico.
• Embolismo Gaseoso : puede presentarse en el paso del C02 a la sangre, pulmón y corazón, siendo una complicación extremadamente rara, se toman las medidas necesarias para prevenirla.
• Flebitis : es la inflamación de las venas utilizadas para la administración de líquidos y medicamentos durante el procedimiento quirúrgico. Con calor local y anti inflamatorios tópicos cede en varios días.
• Infección : una de las mayores ventajas de la cirugía laparoscópica es la menor incidencia de infecciones en comparación con la cirugía abierta, pero de presentarse, es manejada con antibióticos.
• Reacciones Alérgicas : la evaluación pre quirúrgica permite predecir alergias, pero en caso de presentarse, son manejadas médicamente por el anestesiólogo.
• Lesiones Neurológicas : debido a la posición ginecológica durante la cirugía laparoscópica se pueden presentar estiramiento de los nervios de los miembros inferiores con síntomas como adormecimiento y falta de fuerza. Esto es transitorio y se toman medidas para prevenirlos.
• Laparoscopia Fallida : en ocasiones es necesario convertir una laparoscopia en una laparotomía (abrir el abdomen) debido a fibromas o úteros muy grandes o la presencia de adherencias severas que impiden la realización de la totalidad del procedimiento por vía laparoscópica. En estos casos se procede a realizar una Minilaparotomía para completar el procedimiento.
• Muerte : es una posibilidad remota
EMBARAZO ECTOPICO
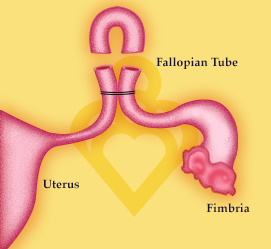
En un embarazo ectópico, el embrión (el óvulo fertilizado) se implanta en un área del tracto reproductivo diferente al útero. Aunque la ubicación más común para un embarazo ectópico es la trompa de Falopio, en raras ocasiones también puede implantarse en el ovario o el abdomen. Los embarazos ectópicos no son viables, lo que significa que el embrión no puede convertirse en un feto saludable, y presentan un peligro grave para el cuerpo de la mujer. Requieren un tratamiento inmediato. Una vez que se termine el tratamiento, el paciente empieza el proceso a veces difícil de recuperación.
Comprende tus opciones de tratamiento. La forma como tú y tu doctor elijan tratar el embarazo ectópico dependerá de tu salud, la ubicación del embarazo ectópico y la extensión del daño existente a tus órganos reproductivos.
- Algunos embarazos ectópicos son eliminados por el cuerpo de la mujer. Si tu embarazo ectópico está en una etapa muy temprana y no tienes síntomas negativos, tu doctor puede recomendar el "manejo expectante" o el "monitoreo activo". Con este proceso, esperas aproximadamente un mes, con una supervisión frecuente del doctor, para ver si tu cuerpo puede resolver el embarazo ectópico sin un tratamiento adicional. En general, este enfoque solo tiene sentido cuando tus niveles de gonadotropina coriónica humana (hCG, por sus siglas en inglés), una hormona que se produce durante el embarazo, son bajos y están bajando o cuando no tienes síntomas.
- Si el embarazo ectópico se diagnosticó muy temprano y no tienes sangrado interno, tu doctor puede sugerir una inyección de metotrexato. El metotrexato detendrá el crecimiento de las células de división rápida, incluyendo el tejido del embarazo (por lo que es importante descartar un embarazo normal). Puede requerirse un par de inyecciones para que este método funcione completamente.
- La salpingostomía laparoscópica es un procedimiento que retira el tejido del embarazo sin retirar ninguna parte de la trompa de Falopio. Este tratamiento generalmente es apropiado para los embarazos ectópicos en etapas tempranas, cuando la trompa de Falopio no se ha roto. La mayoría de los tratamientos quirúrgicos para los embarazos ectópicos usan la laparoscopía, la cual se realiza bajo anestesia general e involucra usar un pequeño tubo con una cámara y una luz que se introduce a través de una pequeña incisión.
- La salpingectomía total puede ser necesaria si la trompa de Falopio está muy dañada, si tienes un sangrado muy intenso o en el caso de un embarazo ectópico grande. En una salpingectomía total, se retira la trompa de Falopio que contiene al embarazo ectópico.
- La laparotomía es una cirugía abdominal que generalmente se requiere en casos de emergencia, como trompas de Falopio rotas o sangrado intenso. Las laparotomías involucran incisiones más grandes y tiempos de recuperación más largos que las laparoscopías.
MI OPINION:
El embarazo ectopico se puede presentar por diferentes factores que influyen a la mujer como:
- Un embarazo ectópico anterior.
- Una enfermedad inflamatoria anterior de la pelvis causada por una enferemedad de transmisión sexual.
- Una infección previa en las trompas de Falopio.
- Una ligadura de trompas que no ha tenido éxito o una inversión de la ligadura de trompas.
- Una intervención quirúrgica abdominal o tubárica con cicatrización postoperatoria.
- Complicaciones tras una operación de apendicitis.
- Una fecundación in vitro.
- Un DIU aún colocado en el momento de la concepción.
- Una endometriosis, una afección que ocasiona que el tejido de la matriz invada y dañe el tejido reproductor circundante.
- El hecho de tomar hormonas, específicamente estrógenos y progesterona, puede hacer más lento el movimiento normal del óvulo fecundado a través de las trompas de Falopio y llevar a un embarazo ectópico.
- La "píldora del día siguiente" (píldora poscoital) ha sido relacionada con varios casos de embarazo ectópico.
- Algunos estudios apuntan a que tal vez, abortos múltiples provocados favorezcan el embarazo ectópico.
- Tal vez la exposición al dietilestilbestrol (DES) en el seno materno (un estrógeno sintético empleado antiguamente en embarazadas), sobre todo si ello ocasionó anomalías en el aparato reproductor.
TERATOMA
Un teratoma es un tumor ovarico de origen embrionario. El término teratoma procede del griego tumor monstruoso.
El diagnóstico definitivo de un teratoma se basa en su histología, un teratoma es un tumor con componentes de órganos que provienen de derivados normales de las tres capas germinativas (endodermo, mesodermo, ectodermo). Raramente, pueden no ser de alguna de esas tres capas la identificación. Los teratomas pueden contener pelo, diente, hueso. Usualmente, un teratoma no contiene ningún órgano, sino uno o más tejidos normalmente encontrados en órganos como cerebro, tiroide, hígado y pulmón.
El teratoma tiene una forma benigna llamada teratoma maduro y una forma cancerosa llamada teratoma inmaduro. El teratoma maduro es, el tumor ovárico de células germinales más frecuente, y por lo general afecta a mujeres en edad fértil (desde adolescentes hasta mujeres entre cuarenta y cincuenta años). A menudo se denomina quiste dermoides, debido a que su revestimiento se asemeja a la piel. Se cura al paciente mediante la extirpación quirúrgica del quiste.
Los teratomas inmaduros se presentan en niñas y mujeres jóvenes, por lo general menores de 18 años. Estos tumores cancerosos poco frecuentes se asemejan a tejidos embrionarios o fetales, tales como el tejido conectivo, las vías respiratorias y el cerebro. Cuando no se han extendido más allá del ovario y la inmadurez no es prominente (teratoma inmaduro de grado 1), se curan mediante la extirpación quirúrgica del ovario.
El teratoma tiene una forma benigna llamada teratoma maduro y una forma cancerosa llamada teratoma inmaduro. El teratoma maduro es, el tumor ovárico de células germinales más frecuente, y por lo general afecta a mujeres en edad fértil (desde adolescentes hasta mujeres entre cuarenta y cincuenta años). A menudo se denomina quiste dermoides, debido a que su revestimiento se asemeja a la piel. Se cura al paciente mediante la extirpación quirúrgica del quiste.
Los teratomas inmaduros se presentan en niñas y mujeres jóvenes, por lo general menores de 18 años. Estos tumores cancerosos poco frecuentes se asemejan a tejidos embrionarios o fetales, tales como el tejido conectivo, las vías respiratorias y el cerebro. Cuando no se han extendido más allá del ovario y la inmadurez no es prominente (teratoma inmaduro de grado 1), se curan mediante la extirpación quirúrgica del ovario.
DIAGNÓSTICO | ||||||||
CISTOADENOMA
Tumor benigno formado por un gran quiste derivado del epitelio glandular ovárico y con secreciones en su interior.
El diagnóstico se realiza generalmente con la ecografía transvaginal practicada en la consulta ginecológica (ver mas sobre revisión ginecológica). Su imagen es la de una estructura circular sonoluscente ( negra ) bien delimitada, sin papilas ni gruesos tabiques en su interior.
Suele ser asintomática o producir molestias pélvicas.
No desaparece con el tratamiento de anovulatorios hormonales.
El tratamiento de elección es la cirugía laparoscópica, con quistectomía si es posible y siempre intentando ser muy conservadores (conocer mas sobre nuestra unidad de laparoscopia).
El diagnóstico de una tumoración anexial constituye uno de los hallazgos más frecuentes que surgen en la práctica clínica diaria. El 85% de estos tumores son benignos y tienen su máxima incidencia entre los 20-44 años.
El CISTOADENOMA es un tumor benigno de ovario derivado del epitelio superficial.
Macroscópicamente es un tumor de contenido líquido similar al suero, superficie lisa y vasos prominentes. El tamaño es variable, desde pocos centímetros hasta grandes masas con tabiques finos y a veces bilaterales.
Suelen ser asintomáticos y de crecimiento lento, por lo que habitualmente se diagnostican en el curso de una exploración ginecológica rutinaria (ver más sobre revisión ginecológica). La intensidad de la clínica va a depender del tamaño, tipo histológico y de la aparición o no de complicaciones (dolor abdominal, aumento del perímetro abdominal, síntomas compresivos como disnea si es muy grande o síntomas por secreción hormonal).
Los pilares principales para el diagnóstico son: el examen pélvico, la ecografía transvaginal (y otras pruebas de imagen) y la determinación analítica de marcadores tumorales, aunque el diagnóstico de certeza será exclusivamente anatomopatológico (tras su extirpación).
La actitud terapéutica dependerá de: la edad, criterios analíticos de benignidad y el tamaño del tumor, y es de elección la cirugía Laparoscópica con Quistectomía, intentando ser muy conservadores. Sólo en la mujer postmenopáusica (cuando ya se ha retirado la menstruación) estará indicada de entrada la cirugía completa (ver más sobre nuestra unidad de Laparoscopia).

MIOMECTOMIA
La miomatosis uterina es el tumor benigno más frecuente en el aparato genital femenino. La prevalencia es de hasta el 50 % en algunas poblaciones y los síntomas aparecen con mayor frecuencia durante la paramenopausia. La mayoría de las mujeres con miomatosis uterina no requieren tratamiento alguno ya que los miomas son frecuentemente asintomáticos, sin embargo cuando son sintomáticos la miomectomía es una opción valedera como tratamiento conservador.
Hasta hace poco tiempo la laparotomía era el abordaje habitual. La primer publicación de miomectomía laparoscópica fue en 1979. Desde entonces los grandes avances en cirugía laparoscópica han hecho que esta técnica sea cada vez más sencilla existiendo hoy múltiples publicaciones que avalan la misma (1).
EVIDENCIAS: MIOMECTOMÍA LAPAROSCÓPICA vs. LAPAROTÓMICA
El valor de la miomectomía laparoscópica como alternativa al tratamiento por laparotomía ha sido evaluado a través de distintos estudios de los que seleccionamos las investigaciones clínicas aleatorizadas (ICAs).
Mais et al realiza una ICA comparando la miomectomía laparoscópica (ML) con la abdominal. Estudios anteriores demostraban que el tiempo operatorio era significativamente mayor en la cirugía laparoscópica cuando la paciente era portadora de más de cuatro miomas con un diámetro promedio de más de 6 cm. Basado en esto, el criterio de inclusión elegido fue que los pacientes fueran portadoras de no más de cuatro miomas , y que el mayor tuviera un diámetro entre 4 y 6 cm. La cirugía laparoscópica se asoció con recuperación postoperatoria más rápida(2).
Seracchioli et al publicaron un estudio randomizado en el cual los pacientes fueron asignados para laparotomía o laparoscopía de acuerdo al siguiente criterio: la paciente debía ser portadora de por lo menos un mioma mayor de 5cm y no presentar más de 3 miomas, ninguna paciente podía presentar una histeromegalia que sobrepasara la cicatriz umbilical. Se utilizó coagulación monopolar y suturas en la cirugía laparoscópica. La mayoría de las pacientes eran portadoras de un mioma único.
Como conclusión no hubo diferencias significativas entre los dos grupos. Los autores tuvieron que convertir de laparoscopía a laparotomía en tres pacientes. En el grupo de laparoscopía tanto la morbilidad postoperatoria como el tiempo de recuperación fue menor. La tasa de embarazos ,abortos, parto pretérmino y cesárea fue la misma para los dos grupos. No se reportó ningún caso de rotura uterina y finalmente la recurrencia de los miomas fue la misma en los dos grupos.(2)
Otros estudios comparativos no randomizados han demostrado también que el tiempo de recuperación postoperatoria de miomectomía laparoscópica es menor. A este respecto Landy et al evaluaron 368 mujeres a las que se realizó ML. El tiempo promedio de la cirugía fue 100.78 +/- 43.83 minutos. La hemoglobina y el hematocrito descendieron en promedio 1.38 +/- 0.93 y 4.8+/- 2.9 g/100 ml respectivamente y la estadía hospitalario fue de 2.89 +/- 1.3 días.
Se reportaron 12 (3.34%) complicaciones intraoperatorias, requiriendo 10 pacientes tranfusión de sangre intraoperatoria. La mayor complicación postoperatoria fue la hemorragia que requirió tranfusión postoperatoria en tres mujeres y una segunda laparoscopía en dos de ellas. Doce pacientes presentaron fiebre en el postoperatorio y no se evaluaron en este estudio la tasa de eventos gestacionales posteriores (2).
TERAPIA HORMONAL PREOPERATORIA
Algunos trabajos plantean el uso de análogos del GnRH en el preoperatorio con el fin de disminuir el tamaño uterino, lográndose una reducción del volumen del mismo entre un 35-50%. Esta reducción se alcanza luego de un tratamiento de 12 semanas y no se obtienen mejoras en los resultados con un tratamiento más prolongados.
En 1998 Zullo realiza una ICA evaluando el uso preoperatorio del GnRH previo a la realización de ML. Un total de 67 pacientes con miomas sintomáticos fueron randomizados en 2 grupos: a uno se le administró durante 2 meses GnRH y al otro no. La pérdida sanguínea y el tiempo operatorio fue significativamente menor en pacientes que habían recibido GnRH. Sin embargo en el grupo que recibió GnRH y eran portadores de miomas ecograficamente hipoecogénicos el tiempo operatorio fue significativamente mayor. Esto se debió a que la enucleación del mioma resultó más dificultosa debido a una distorsión de los planos de clivaje y a un aumento de la hialinización.
Campo realiza otro estudio randomizado sobre un total de 60 pacientes concluyendo que el tiempo operatorio fue significativamente mayor en el grupo que recibió GnRH ( 157 vs. 112 min, P= 0.01) sumado al hecho de que muchas pacientes manifestaron sindrome climatérico(1)
Palomba en febrero de 2001 publica una ICA valorando si el agregado de Tibolona a la terapia preoperatoria con GnRH mejora los resultados del uso exclusivo de esta última, concluyendo que no hay cambios en cuanto a la pérdida sanguínea ni al tiempo operatorio con esta asociación (3).
CONSIDERACIONES TÉCNICAS
La ML consiste en tres fases : escisión del mioma, reparación del miometrio y extracción de la pieza.
ESCISIÓN DEL MIOMA
Los miomas pediculados no plantean mayores dificultades. Los miomas subserosos sesiles y los intramurales son los más dificultosos. En general la primer etapa consiste en la inyección en la serosa de vasopresina que disminuye el sangrado intraoperatorio aunque pueden pasar desapercibidas zonas que más tarde ocasionen sangrado. Además tiene graves complicaciones sistémicas si se inyecta intravascular en forma accidental.
El próximo paso es la incisión de la serosa. No hay consenso si ésta debe ser vertical u horizontal, y hay autores que defienden una u otra técnica argumentando los dos grupos que facilita la sutura laparoscópica mejorando el cierre miometrial.
El lecho debe ser coagulado con bisturí bipolar teniendo la precaución de no coagular en forma extensa ya que predispone a la necrosis, dificulta la cicatrización y puede predisponer a rotura uterina posterior.(1)
REPARACIÓN DEL MIOMETRIO
Si se trata de un mioma pequeño y superficial y la paciente no desea futuros embarazos los bordes del defecto uterino son hemostasiados sin cierre miometrial. Sin embargo si la paciente desea futuros embarazos, el miometrio debe ser suturado en varios planos con sutura reabsorbible. Por este motivo la ML debe reservarse para los endoscopistas más familiarizados con la técnica de sutura endoscópica.(1)
Puede instilarse azul de metileno en la cavidad uterina para corroborar la indemnidad del endometrio.
EXTRACCION DE LA PIEZA
Con el advenimiento de la técnica de ML, la extracción de la pieza ha cobrado especial interés, dado que muchas veces es responsable de la prolongación del tiempo operatorio perjudicando el costo beneficio de la cirugía laparoscópica . Cualquiera sea la técnica de remoción de la pieza, ésta no debe comprometer la seguridad del paciente ni en el intra ni en el postoperatorio.
Se realizó una revisión sistemática del tema, publicada en agosto de 2001en Curr Opin Obstet Gynecol.(4)
Dado que en la mayoría de los casos no es posible extraer la pieza de miomectomía a través de la incisión realizada para un trócar de 5 mm, es necesario ampliar la misma, con lo que la posibilidad de hernias se incrementa.
Previo al surgimiento del morcelador de Storz la extracción de piezas grandes requería la reducción de la misma con tijera y extracción en múltples veces, lo que convertía al procedimiento en tedioso y aumentaba el riesgo de daño de la fascia y de las consiguientes hernias, a pesar del cierre rutinario de la fascia.(4)
Actualmente no se han reportado la aparición de hernias y esto se atribuye fundamentalmente a la aparición y uso de morceladores que permite transformar el mioma en trozos pequeños que se extraen sin dificultad. De todas formas no está exenta de riesgos, ya que es un instrumento con alto poder de corte y hay que ser cauteloso para no dañar tejidos vecinos.
SUTURA BARBADA
Desde el inicio de la cirugía las suturas se han asegurado mediante la realización de un nudo. A pesar de la multitud de materiales usados, no existe evidencia acerca de cuál es la mejor sutura y su forma de anclado óptima. Históricamente, en la realización de una sutura se asume que su fijación debe hacerse mediante anudado final. Para la mayoría de los cirujanos resulta difícil comprender una sutura sin su nudo acompañante. Recientemente se han introducido en el mercado suturas barbadas que permiten la realización de una sutura sin anudado final. Esta revisión pretende analizar las ventajas, seguridad y aplicaciones en el uso de las suturas barbadas. Para ello, se ha realizado un análisis de aquellos artículos relevantes, obtenidos a través de una búsqueda bibliográfica en la base de datos MEDLINE, entre los años 2000 y 2014, empleando como palabras clave: «barbed suture», «laparoscopic anastomosis», «laparoscopic knots».
En 1956, Alcamo patenta la primera sutura barbada unidireccional1. Su uso preliminar se publicó en 1967 para la reparación de tendones flexores de la mano2.
Conceptos sobre propiedades de las suturas
La idea de realizar una sutura sin anudado final puede resultar de una dudosa seguridad para muchos cirujanos. Sin embargo, la realización del nudo quirúrgico, aunque ampliamente aceptada por la tradición quirúrgica, tiene algunos inconvenientes:
Estudios experimentales
Para un cirujano no resulta fácil, al menos inicialmente, realizar una sutura y no anudarla sin que le surjan dudas acerca de la seguridad. El método de confección de la sutura barbada implica la realización de pequeños cortes en la superficie de una sutura lisa, lo que a efectos clínicos podría implicar una reducción de la fuerza tensil como consecuencia de la disminución del «diámetro funcional» de la sutura10. Sin embargo, los datos existentes indican que la sutura barbada presenta una fuerza tensil comparable a la de su equivalente sin barbar tal y como reportan diversos estudios in vitro
Uso de las suturas barbadas en cirugía
La sutura barbada se ha utilizado durante los últimos años en diferentes especialidades. En ginecología, diferentes artículos se han publicado aconsejando el uso de la sutura barbada para reducir el tiempo operatorio, incluso en algunos casos, el sangrado intraoperatorio. Tanto en la realización de miomectomía, como histerectomía, diferentes autores defienden su uso al facilitar la técnica quirúrgica. En el campo de la urología, exceptuando algún autor que publica resultados desfavorables con el uso de esta sutura (alto índice de estenosis ureteropélvica en una serie corta [5/6 pacientes]), la gran mayoría de los urólogos defienden su uso por la disminución del tiempo operatorio y la seguridad en las anastomosis
Con relación a la cirugía general, la gran mayoría de publicaciones está en relación con la cirugía bariátrica y su uso en el bypass gástrico laparoscópico. Es bien sabido que la realización de la anastomosis intracorpórea (sutura y anudado) requiere una destreza y habilidad importantes por parte del cirujano. De ahí, que todo lo que pueda facilitar y hacer más reproducible y segura la anastomosis será valorado por la gran mayoría de especialistas
 FECUNDACIÓN IN VITRO
es una técnica por la cual la fecundación de los ovocitos por los espermatozoides se realiza fuera del cuerpo de la madre. La FIV es el principal tratamiento para la esterilidad cuando otros métodos de reproducción asistida no han tenido éxito. El proceso implica el control hormonal del proceso ovulatorio, extrayendo uno o varios ovocitos de los ovarios maternos, para permitir que sean fecundados por espermatozoides en un medio líquido. El ovocito fecundado puede entonces ser transferido al útero de la mujer, en vistas a que anide en el útero y continúe su desarrollo hasta el parto.
El término in vitro es un término en latín que significa ‘en cristal’. Se utiliza porque en los primeros experimentos biológicos en los que se realizaban cultivos de tejidos fuera de los organismos vivos de los cuales procedían, se realizaban en contenedores de cristal, tales como tubos de ensayo, probetas o placas de Petri. En la actualidad, el término in vitro se refiere a cualquier procedimiento biológico que se realiza fuera del organismo en el que tendría lugar normalmente, para distinguirlo de un experimento in vivo donde el tejido permanece dentro del organismo vivo en el que normalmente se encuentra. Coloquialmente, a los bebés concebidos a través de FIV se les denomina bebés probeta, refiriéndose a contenedores de cristal o plástico denominados probetas, que se utilizan frecuentemente en los laboratorios de química y biología. Sin embargo, normalmente la fecundación in vitro se realiza en placas planas denominadas placas de Petri; las placas de Petri utilizadas más a menudo están producidas en plástico, sin embargo, el nombre FIV sigue conservándose.
INSEMINACIÓN ARTIFICIAL Inseminación artificial es todo aquel método de reproducción asistida que consiste en el depósito de espermatozoides en la hembra mediante instrumental especializado y utilizando técnicas que reemplazan a la copulación, implantándolos en el útero, en el cérvix o en las trompas de Falopio, con el fin de lograr la gestación.
Los sumerios, además de inventar la escritura, registraron por primera vez una técnica, muy artesanal por lo demás, de inseminación artificial en ovinos, la misma que se utilizó posteriormente en equinos.
Pese a la creencia de que la inseminación artificial es una tecnología moderna, los primeros intentos de llevarla a cabo se remontan al siglo XV: se cree [cita requerida] que la inseminación artificial fue intentada por Juana, esposa del Rey Enrique IV de Castilla (conocido como "el impotente"). En 1677 el científico holandés Leeuwenhoek observó espermatozoides gracias a los microscopios que había construido. Más de 100 años después, el sacerdote y fisiólogo italiano Lazzaro Spallanzani demostró que debía existir contacto físico entre el huevo y el esperma para que se desarrollara un embrión. Hasta ese momento se creía que el embrión era "producto de la semilla masculina, nutrido en el suelo de la mujer". Spallanzani realizó experimentos exitosos de inseminación artificial en peces y anfibios. En 1784 practicó la primera inseminación artificial de una perra, lo que derivó en el nacimiento de tres cachorros totalmente sanos 62 días más tarde.
En 1790 el cirujano escocés John Hunter recogió en una jeringa caliente el semen de un comerciante con hipospadia y lo inyectó en la vagina de su mujer, realizando la primera inseminación artificial en un ser humano en la historia.1 La idea de conservar el semen masculino se remonta a 1866 cuando Paolo Mantegazza creó en Pavía un banco de esperma veterinario. Los esfuerzos para desarrollar técnicas modernas de inseminación artificial comenzaron en Rusia en 1899. Se tiene constancia {Ivanoff, 1922} de la inseminación artificial de un caballo realizada con éxito en 1922. Hacia el año 1950, la inseminación artificial se convirtió en una industria establecida: en 1949 aparecieron métodos de congelación y descongelación del esperma y en 1950 surge la idea de añadir antibióticos al semen para prevenir enfermedades venéreas. Posteriormente, en los años 70 y 80 se desarrollaron métodos eficaces de recolección de semen.
El semen bovino congelado en nitrógeno líquido (-196 °C) ha permitido su almacenamiento por largos períodos (el más antiguo desde 1952 a la fecha) sin que se produzca un deterioro en la fertilidad del mismo. Gracias a ello el semen (y la genética en él contenida) se conserva, se transporta y se utiliza en muy diversos ambientes.
POMEROY
El POMEROY es el tipo de LIGADURA DE TROMPAS, o ESTERIZACIÓN TUBÁRICA más frecuentemente realizada en el mundo. El POMEROY SÍ PERMITE RECONSTRUIR LAS TROMPAS.
Se puede hacer mediante una incisión de dos a cuatro centímetros, en la parte baja del abdomen, inmediatamente encima del pubis, cuando la matriz está de tamaño normal (más de dos meses después de un parto). Es la técnica más popular en las campañas de planificación y se anota como POMEROY POR MINILAPAROTOMIA.
También se puede hacer inmediatamente después de un parto vaginal mediante una incisión pequeña en el ombligo. Tanto en este caso, como en el anterior de POMEROY POR MINILAPAROTOMÍA, es muy difícil intentar otro tipo de ligadura de trompas a través de esas incisiones pequeñas, razón por las cuales cuando se encuentran las cicatrices de estas incisiones es muy seguro que en realidad lo que se practicó sí fue un POMEROY.
En una cesárea es la técnica de esterilización más frecuentemente utilizada. Sin embargo es necesario asegurarse revisando la descripción de la cirugía (nota operatoria o descripción quirúrgica), ya que en ese momento pueden hacer POMEROY o utilizar una técnica mucho más agresiva como es el corte de la parte final de la trompa (fimbria), lo que la inutilizaría para una reconstrucción de trompas convencional.
En esta técnica quirúrgica tradicional del POMEROY se levanta la sección 2 de la trompa y se anuda por debajo con una sutura (hilo quirúrgico) que se reabsorbe días después.
|





No hay comentarios.:
Publicar un comentario